Le contrôle qualité de la Radiothérapie dans les études cliniques

La place de la Radiothérapie en Oncologie
Retrouvez la version intégrale de notre webinaire du 07 juillet sur le sujet.
Il vous suffit de vous inscrire pour la visionner.
En 2018, il y a eu plus de 18 millions de nouveaux cas de cancer dans le monde. Les prévisions montrent que ce nombre devrait malheureusement continuer à augmenter pour atteindre 27,5 millions de cas en 2040 i.

La prise en charge des cancers est multidisciplinaire, associant principalement chirurgie, chimiothérapie et radiothérapie. La radiothérapie reste le traitement principal, utilisé pour plus de 50 % des patients.
Par contre, selon l’étude “Characteristics of radiotherapy trials compared with other oncological clinical trials in the past 10 years” ii parue en 2018, les études interventionnelles de radiothérapie ne représentent que 5,3% des essais en oncologie sur la période 2006-2016. L’une des explications viendrait des plus grandes difficultés de financement de ces études, alors qu’elles sont pourtant nécessaires afin d’évaluer les nouvelles techniques de radiothérapie.
Cependant, selon “Overview of ongoing clinical trials investigating combined radiotherapy and immunotherapy” iii paru en 2018, la place de la radiothérapie est plus importante dans les essais d’immunothérapie. L’association radiothérapie et immunothérapie dans les études augmente ces dernières années et cela devrait continuer dans les années à venir.
Enfin, si l’on regarde toutes les études d’oncologie publiées dans ClinicalTrial.gov, près de 25% de ces études intègrent de la radiothérapie, que ce soit dans l’objectif principal du traitement ou non. Même si on estime que ClinicalTrial.gov ne référence que 70 % des études, cette proportion semble réaliste.
Les chiffres clés :
- La radiothérapie est utilisée dans le traitement de plus de 50 % des patients.
- Les études de radiothérapie ne représentent que 5,3% des essais en oncologie.
- On trouve de la radiothérapie dans environ 25% des essais cliniques d’Oncologie.
La Radiothérapie aujourd’hui
La radiothérapie a connu une évolution majeure ces dernières années, notamment pour mieux cibler, pour mieux suivre la tumeur et pour mieux adapter le traitement du patient, avec des machines qui intègrent majoritairement de l’imagerie embarquée comme l’IRM et le Scanner pour s’assurer que le traitement prévu est bien celui réalisé.
La radiothérapie reste néanmoins un traitement complexe nécessitant différentes étapes :
- Imagerie : pour définir où traiter, faisant appel de plus en plus à l’imagerie multimodalité
- Planification : comment traiter la tumeur en évitant les organes à risques (OARs)
- Traitement : afin de délivrer ce qui a été prévu sur l’ensemble des séances
Cette complexité de prise en charge en radiothérapie va être plus difficile à harmoniser dans les études et les problèmes à résoudre résident principalement dans la variabilité inter-opérateurs et inter-centres :
- Le respect des recommandations de contourage : est-ce que la tumeur et les organes à risque sont définis et contourés de la même manière dans tous les centres ?
- Le respect des contraintes dosimétriques : est-ce que tous les centres traitent bien selon le même protocole et avec les mêmes contraintes dosimétriques.
Sans l’harmonisation et la standardisation des traitements entre les différents patients, les résultats obtenus ne pourront pas être correctement évalués et analysés. Cela est en particulier l’un des objectifs principaux du rapport mis en avant par ICRU en 2013 iv.
Les impacts d’une déviation du protocole dans les essais cliniques
En 2013, l’étude “Radiotherapy Protocol Deviations and Clinical Outcomes: A Meta-analysis of Cooperative Group Clinical Trials“ v montre l’impact des déviations au protocole sur la qualité et le résultat des études. Cette analyse a été réalisée sur 8 études menées par des groupes coopérateurs reconnus. Dans cette publication, des déviations par rapport au protocole ont été observées dans 8 à 71% des cas (médiane à 32%). Ces déviations ont montré un impact important sur les résultats observés, que ce soit pour la survie des patients ou pour les objectifs secondaires de l’étude.
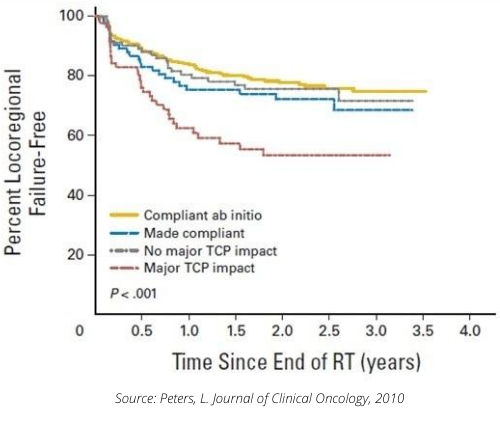
En particulier, l’étude “Critical Impact of Radiotherapy Protocol Compliance and Quality in the Treatment of Advanced Head and Neck Cancer : Results From TROG 02.02“ vi, réalisée en 2010, évalue l’impact de la qualité du traitement dans une étude ORL de phase III avec 861 patients sur 82 centres répartis dans 16 pays. Cette étude avait déjà un contrôle qualité et une revue centralisée des plans de traitements. A postériori, il y a eu une revue centralisée des plans délivrés pour tous les patients en mettant d’un côté les 612 patients que l’on considérait comme « protocol compliant », évalués principalement par rapport à la dosimétrie, et de l’autre côté les 208 patients « non compliant ». Chez ces derniers patients, un expert indépendant était chargé de les séparer en deux groupes : ceux pour lesquels la déviation au protocole avait un impact estimé sur le traitement et ceux pour lesquels la déviation n’aurait pas d’impact.
Les résultats montrent des courbes de survies et de récidives très différentes entre les groupes. On voit que les patients classés en déviation majeure ont une courbe de survie différente de celle des autres patients.
Il a également été noté que la réponse à l’étude aurait été différente si l’on comparait les résultats entre les patients ayant reçus une « Bonne radiothérapie » et ceux ayant eu une « Mauvaise radiothérapie ».
Le besoin principal qui a été exprimé dans cette étude était d’avoir un contrôle qualité en temps réel et donc, qu’il soit réalisé en prospectif, avant le traitement du patient.
Le sujet reste d’actualité, notamment avec l’étude menée en 2018 “Quality of radiotherapy reporting in randomized controlled trials of prostate cancer“ vii.On y trouve une revue de 59 essais cliniques concernant la prostate de 1987 à 2016. Les auteurs ont analysé 10 critères qu’ils pensaient important pour la qualité des traitements. L’étude était considérée comme bonne si 7 critères étaient respectés. Seul 40 % des essais y répondaient.
Dans une autre étude ORL de 2019, “The impact of clinical trial quality assurance on outcome in head and neck radiotherapy treatment“ viii, les auteurs ont défini des index de qualité sur le contourage du volume cible, sur le contourage des organes à risque et sur la couverture dosimétrique. Ils ont alors créé un score nommé « RTQA score » qu’ils ont ensuite analysé au regard des résultats cliniques. On retrouve également dans cette étude un impact sur les différentes courbes de survie des patients ayant un mauvais score RTQA.
On voit bien, dans ces différentes études, l’importance et l’intérêt de faire un contrôle qualité rigoureux de la radiothérapie dans les études cliniques d’Oncologie.
Bien sûr, ce contrôle qualité à un coût, principalement humain pour revoir les dossiers, mais il est nécessaire pour la qualité des traitements et la pertinence des résultats obtenus dans les étudesix. A ce titre, de nombreuses revues n’acceptent plus de manuscrit si la méthodologie du contrôle qualité de la radiothérapie n’a pas été décrite et documentée.
“Although the incorporation of an RT-QA program may be a costly initial component of clinical trials, in the long term we cannot afford to run trials dependent on high-quality RT without it.”
Source: McDowell L., IJROBP, 2018
Les solutions à mettre en place sont connues
Radiation Therapy Quality Assurance (RTQA). De nombreuses recommandations ont été publiées, comme celles de l’AAPM x ou du « Global Harmonisation Group » xi, qui regroupe des sociétés savantes et des groupes coopérateurs sur le plan international et qui recommande en particulier :
- La mise en place de Dummy Runs, c’est-à-dire d’exercices de contourage, de dosimétrie, voire de recalage sur un cas clinique fictif afin de s’assurer que chaque centre investigateur a bien intégré l’ensemble du protocole de traitement de l’étude.
- Une fois que le centre a été « approuvé » sur la base des Dummy Runs, ils préconisent une revue centralisée des plans avant le traitement de tous les patients, des premiers patients de chaque centre ou sur des patients tirés au sort.
Les solutions AQUILAB pour l’AQ RT dans les essais cliniques
AQUILAB est impliqué depuis de nombreuses années dans l’amélioration de la qualité et l’harmonisation de la radiothérapie dans les essais cliniques. Notre expertise et nos solutions technologiques permettent une mise en place simplifiée des protocoles d’assurance qualité par les promoteurs.
En particulier, notre solution Onco Place est une plateforme web qui permet :
- De gérer les participants de l’essai clinique. On y retrouve un espace investigateur, un espace promoteur et un espace expert. Ces trois espaces sont distincts mais en connexion les uns avec les autres afin de permettre de coordonner le workflow entre les différents participants.
- D’anonymiser, structurer et centraliser les données DICOM / DICOM RT (images, structures, plans et doses) nécessaires aux étapes de contrôle qualité.
- D’analyser les images, les contours et les plans de traitement de tous les TPS du marché grâce aux outils de revue de notre solution ARTIVIEW.
Selon le protocole de l’étude, chaque projet peut être personnalisé afin d’assurer un suivi adapté des inclusions tout en garantissant la sécurité des informations échangées.
Vous pouvez retrouver une démonstration de la plateforme Onco Place lors de la deuxième partie de notre webinaire sur le contrôle le contrôle qualité centralisé de la radiothérapie dans les études cliniques.

Bibliographie
i Global Cancer Observatory. https://gco.iarc.fr/
ii Liu, X., Zhang, Y., Tang, L. L., Le, Q. T., Chua, M. L. K., Wee, J. T. S., … Ma, J. (2018).
Characteristics of radiotherapy trials compared with other oncological clinical trials in the past 10 years.
JAMA Oncology, 4(8), 1073–1079. https://doi.org/10.1001/jamaoncol.2018.0887
iii Cushman, T. R., Caetano, M. S., Welsh, J. W., & Verma, V. (2018).
Overview of ongoing clinical trials investigating combined radiotherapy and immunotherapy.
Immunotherapy, 10(10), 851–859. https://doi.org/10.2217/imt-2018-0019
iv Grégoire, V., & Mackie, T. R. (2011).
State of the art on dose prescription, reporting and recording in Intensity-Modulated Radiation Therapy (ICRU report No. 83).
Cancer/Radiotherapie, 15(6–7), 555–559. https://doi.org/10.1016/j.canrad.2011.04.003
v Ohri, N., Shen, X., Dicker, A. P., Doyle, L. A., Harrison, A. S., & Showalter, T. N. (2013).
Radiotherapy Protocol Deviations and Clinical Outcomes: A Meta-analysis of Cooperative Group Clinical Trials.
JNCI Journal of the National Cancer Institute, 105(6), 387–393. https://doi.org/10.1093/jnci/djt001
vi Peters, L. J., O’Sullivan, B., Giralt, J., Fitzgerald, T. J., Trotti, A., … Rischin, D. (2010).
Critical Impact of Radiotherapy Protocol Compliance and Quality in the Treatment of Advanced Head and Neck Cancer: Results From TROG 02.02.
Journal of Clinical Oncology, 28(18), 2996–3001. https://doi.org/10.1200/JCO.2009.27.4498
vii Soon, Y. Y., Chen, D., Tan, T. H., & Tey, J. (2018).
Quality of radiotherapy reporting in randomized controlled trials of prostate cancer.
Radiation Oncology, 13(1), 1–8. https://doi.org/10.1186/s13014-018-1053-7
viii Zhong, H., Men, K., Wang, J., van Soest, J., Rosenthal, D., Dekker, A., … Xiao, Y. (2019).
The impact of clinical trial quality assurance on outcome in head and neck radiotherapy treatment.
Frontiers in Oncology, 9(AUG), 1–7. https://doi.org/10.3389/fonc.2019.00792
ix McDowell, L. J., & Corry, J. (2018).
A Call to Arms: Radiation Therapy Quality Assurance in the Next Generation of Clinical Trials.
International Journal of Radiation Oncology Biology Physics, 102(5), 1590–1591. https://doi.org/10.1016/j.ijrobp.2018.07.2001
x AAPM Report 113, T. G. (2018).
Guidance for the Physics Aspects of Clinical Trials. https://doi.org/10.37206/172
xi Melidis, C., Bosch, W. R., Izewska, J., Fidarova, E., Zubizarreta, E., … Hurkmans, C. W. (2014)
Radiation therapy quality assurance in clinical trials – Global harmonisation group.
Radiotherapy and Oncology, 111(3), 327–329. https://doi.org/10.1016/j.radonc.2014.03.023